背景介绍
临床现象:干扰素调节因子IRF4在脂肪细胞脂代谢的过程中起重要作用,但在脂肪组织巨噬细胞(ATM)中的作用并不清楚。
科学问题:IRF家族分子IRF4是否调控了ATM的功能?
分子机制研究切入点:
根据是否促进炎症反应,可将巨噬细胞分为M1型和M2型。M1型巨噬细胞分泌IL-1b、TNF-a等促炎分子,而M2型巨噬细胞分泌IL-10等抑炎因子。如果M1型巨噬细胞在脂肪组织中大量聚集,则会引起胰岛素抵抗和代谢功能失调,而M2型则相反。本文从巨噬细胞的两种分型入手,对分子机制进行了解释。
研究对象:
其一,干扰素调节因子4(IRF4),介导先天性免疫反应,激活干扰素下游分子的表达,是脂肪细胞脂代谢过程中的重要转录调控因子。
其二,M2型巨噬细胞,分泌IL-10等抑炎因子,对胰岛素信号通路、脂代谢等过程起促进作用。
本文从IRF4入手,研究了IRF4的缺失对巨噬细胞炎症反应和胰岛素抵抗的影响。机制方面,作者发现IRF4可以促进M2型巨噬细胞的分化,进而抑制脂肪组织巨噬细胞的炎症反应和胰岛素抵抗的发生。
文章思路精要
热点与临床结合:IRF4可以说是转录调控分子中的新明星,本文的通讯作者在2014年发表的一篇Cell文章正是发现IRF4在热基因表达和能量代谢中的关键转录调控作用。因此将IRF4与胰岛素抵抗反应结合,提高了本文的影响力。
体内外共同验证:在表型方面,本文利用了体内外共同验证,体外采用两种巨噬细胞,以及共培养等技术手段,体内则检测了一系列代谢相关的指标。在机制方面,本文同样在体内和体外分别证明了IRF4对M2型巨噬细胞的促进作用。但从文章的完整性来看,机制略显单薄,只看到M2的分化情况还不足以完全解释IRF4的调控作用,这正是本文的主要缺陷。
研究内容
1.提出现象,抛出疑问:
为了验证IRF4在巨噬细胞中的作用,作者分别采用两种不同的小鼠原代巨噬细胞PM(腹腔来源的巨噬细胞)和BMDM(骨髓来源的巨噬细胞),利用TLR4刺激剂和饱和脂肪酸棕榈酸对细胞进行刺激后发现,这些刺激都可以引起巨噬细胞中IRF4的上调表达,这提示IRF4可能参与了巨噬细胞信号通路的调节。
2.选择模型,验证现象:
那么IRF4是在巨噬细胞中的作用到底如何?为此,作者选择了IRF4基因缺失的小鼠,分离小鼠的PM并进行棕榈酸刺激,观察到IRF4缺失后,棕榈酸引起的炎症反应明显加强了。而在小鼠巨噬细胞系中过量表达IRF4,情况却恰好相反。这些结果证明,IRF4可以抑制棕榈酸引起的巨噬细胞中的炎症反应。
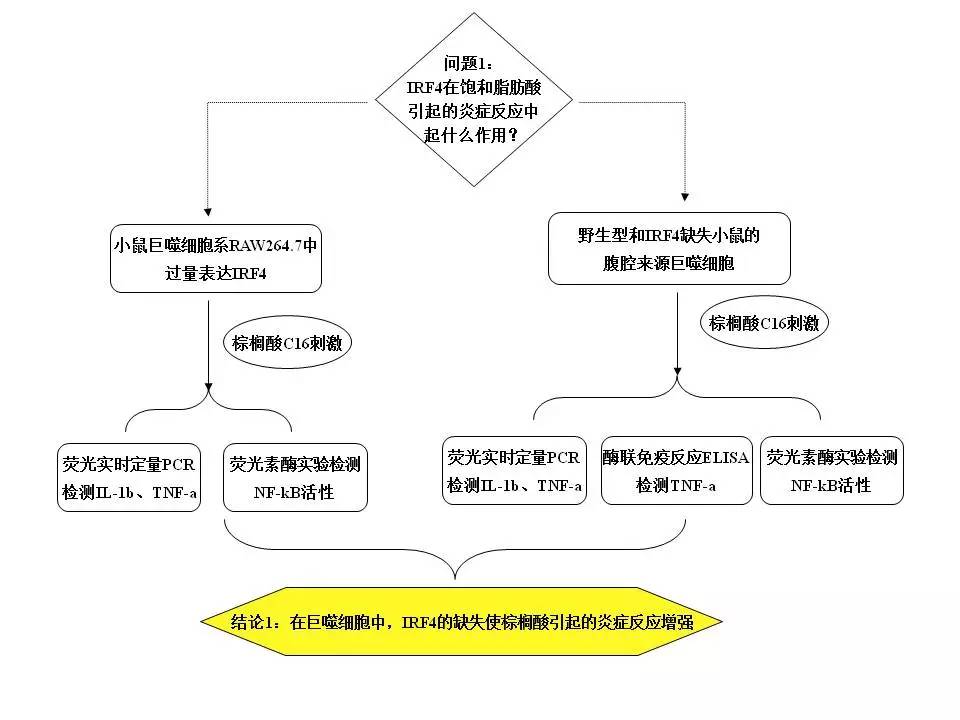
3.细化模型,层层深入:
IRF4的缺失引起了巨噬细胞炎症反应的加强,这对胰岛素抵抗会有影响吗?为此,作者通过将IRF4缺失小鼠的PM与脂肪细胞3T3-L1共培养后,检测脂肪细胞对胰岛素引起的葡萄糖吸收的影响,同时观察胰岛素信号通路中的IRS1和Akt分子的磷酸化水平。结果证明,巨噬细胞中IRF4的缺失使脂肪细胞产生了胰岛素抵抗。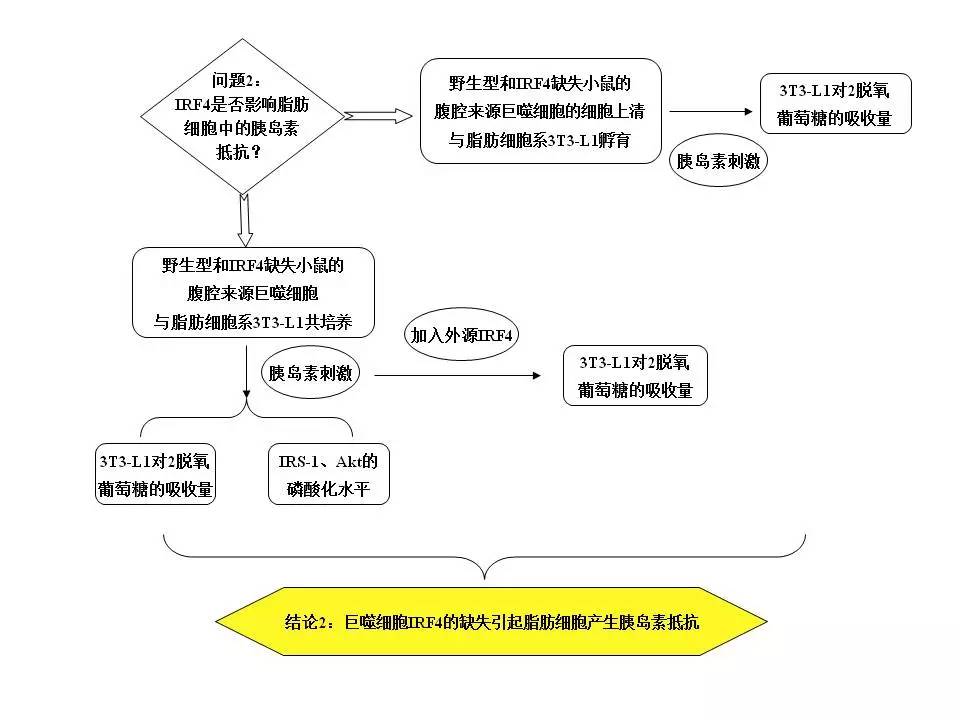
4.病理检测,提升意义:
体内IRF4的缺失会怎样影响小鼠的胰岛素抵抗反应?为了解答这个问题,作者在骨髓中特异性敲除IRF4。发现骨髓缺失IRF4后,小鼠的白脂肪组织中巨噬细胞的浸润明显增多,肝脏、骨骼肌、脂肪组织中的炎症因子大量表达,胰岛素诱导的Akt的磷酸化也明显减弱。这证明IRF4对小鼠体内多器官系统性的胰岛素抵抗都具有抑制作用。
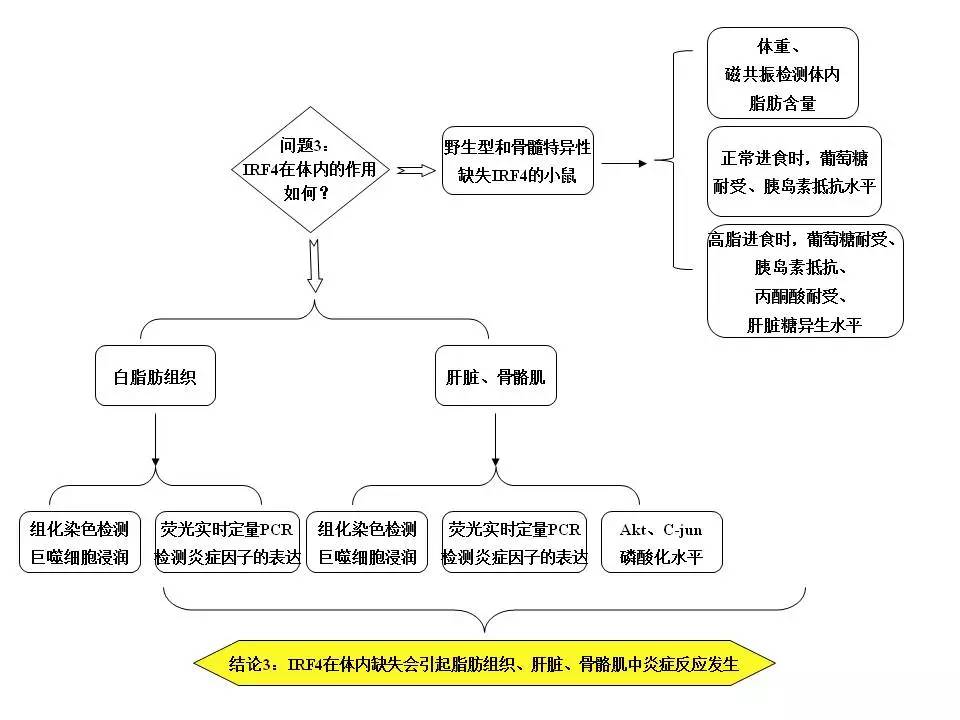
IRF4是如何调控小鼠胰岛素抵抗和炎症反应发生的呢?由于M1型和M2型巨噬细胞在炎症反应中的不同作用,作者推测IRF4可能影响了巨噬细胞的分化。为此,作者检测了IRF4缺失后,脂肪组织巨噬细胞中M1和M2的比例,发现M2明显减少。此外,M1型巨噬细胞相关的炎症因子也明显上调表达。为了验证这一现象,作者在体外的BMDM中进行了不同的刺激,得到了类似结果,即IRF4可以促进M2型巨噬细胞的分化。因此,IRF4通过促进M2型、抑制M1型巨噬细胞,抑制胰岛素抵抗和体内炎症反应的发生。
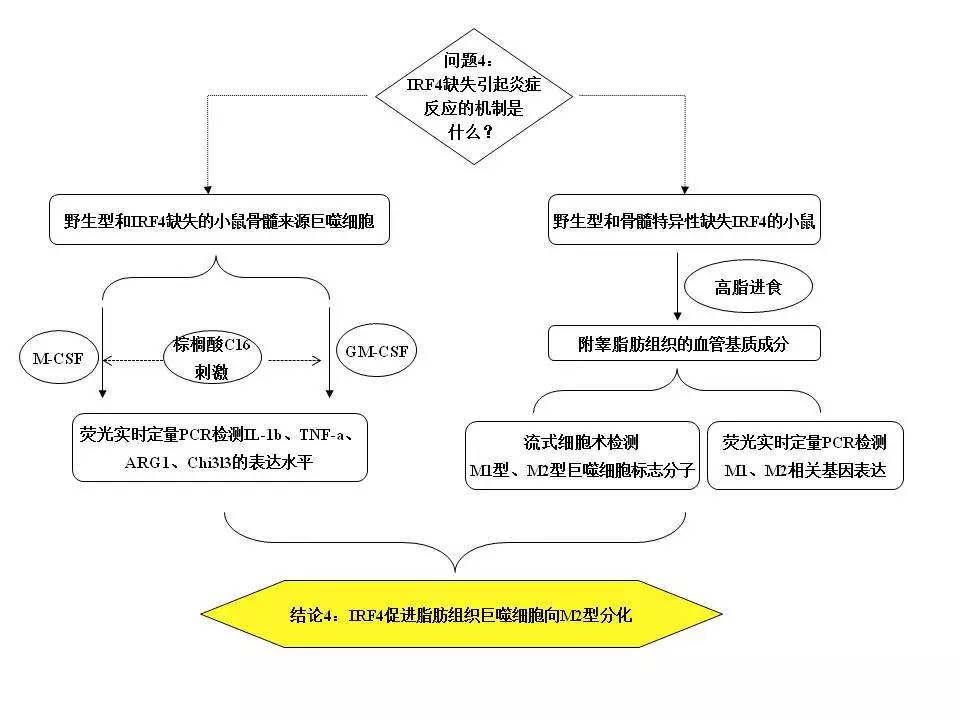
思路总结
肥胖引起机体产生胰岛素抵抗,而炎症反应在此过程中至关重要。IRF家族分子在代谢过程中的作用日益增强,之前的文章证明IRF9在胰岛素抵抗和脂肪肝发生过程中的调控作用。本文关注另外一个IRF家族分子IRF4,研究它在巨噬细胞炎症反应中的作用,并深入到体内的胰岛素抵抗过程中的作用,与IRF9文章思路和结构较为类似:
(1)现象出发:本文首先在巨噬细胞中观察到脂肪酸可以引起IRF4的高表达,这提示IRF4可能具有负反馈调控的作用。
(2)小鼠模型:本文采用骨髓特异性敲除IRF4的小鼠,排除了其他组织器官IRF4对代谢结果的干扰。
(3)结合病理:本文检测了小鼠白脂肪组织、骨骼肌、肝脏中的炎症反应水平,以及体内葡萄糖耐受、胰岛素抵抗等指标,使得IRF4的调控功能更具生理意义。
(4)深入机制:在机制研究中,作者发现IRF4诱导体内M2型巨噬细胞的分化,结合以前的报道结果,M2对炎症反应起到抑制作用,因此推测IRF4对胰岛素抵抗和体内炎症的抑制作用正是通过M2型巨噬细胞发挥的。
编者推荐:本文依据科学现象中的可疑点,再通过体内外验证,从而在分子水平、细胞水平和动物水平上,全方位地确凿论点。关于胰岛素抵抗的分子调控,敬请关注接下来将会发布的几篇文献,以便把握作者完整的研究套路。
原作者介绍:Evan D. Rosen是哈佛医学院波士顿贝斯以色列女执事医疗中心的教授。自2002年至今,在Pubmed数据库检索到该作者以通讯作者身份发表文章19篇。主要杂志包括:Cell、NatCell Biol、J Clin Invest、ProcNatl Acad Sci、Diabetes等杂志。
Evan D. Rosen实验室主要关注脂肪细胞的分化和代谢过程中的分子调控机制,特别在胰岛素抵抗、脂肪细胞代谢等过程中,他们利用转录组学和表观遗传学技术发现了很多关键的调控分子。
来源:解螺旋专家团队编译
2015-07-22